 東京医科大学,国立遺伝学研究所の研究グループは,ALSの運動ニューロンで塊を形成することが知られているTDP-43に,青い光を吸収すると塊を形成するように改変を加え,塊の形成を光照射によって自在に調節する技術を開発した(ニュースリリース)。
東京医科大学,国立遺伝学研究所の研究グループは,ALSの運動ニューロンで塊を形成することが知られているTDP-43に,青い光を吸収すると塊を形成するように改変を加え,塊の形成を光照射によって自在に調節する技術を開発した(ニュースリリース)。
ALS(筋萎縮性側索硬化症)は,知性や五感が保たれたまま全身の筋肉が徐々に衰え,発症から平均2~3年で死に至る神経難病。10万人におよそ2人の割合で発症することが知られており,日本では,約9,200人がこの病気を患っている。
ALSは,筋肉を収縮させる「運動ニューロン」と呼ばれる神経細胞が変性することで発症する。90%以上のALSは,家族や近親者にALSを患った人がいない孤発性とよばれるタイプであり,1つの遺伝子変異が原因ではないため,発症の仕組みの解明が特に遅れている。
14年前に,孤発性ALSの運動ニューロンに形成される塊の主成分が,TDP-43というタンパク質であることが発見された。しかし,体の奥深くにある運動ニューロンのTDP-43を研究することは非常に困難であり,TDP-43の塊と運動ニューロンの変性の因果関係を検証するには至っていなかった。
研究グループは,光照射によって塊の形成を調節できる改変型ヒトTDP-43を開発し,ALSの状態によく似た運動ニューロンの異常を,モデル生物ゼブラフィッシュの生体内で再現することに成功した。
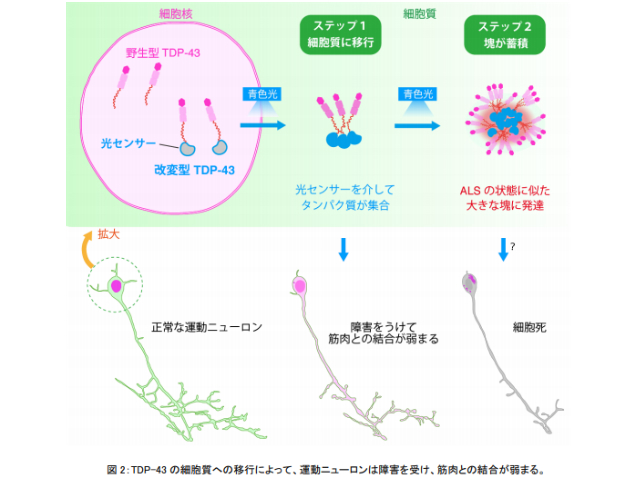
TDP-43の塊の形成は,タンパク質の集合による「細胞核から細胞質への移行」,「細胞質における塊の形成」の2つのステップからなることが明らかになった。このうち,光の照射量を調節して「細胞核から細胞質への移行」を誘発するだけでも,運動ニューロンが萎縮し,筋肉との結合が弱くなることがわかった。さらに,長期にわたって光を照射し続けると,泳ぐことが困難になる魚が現れた。
運動ニューロンは,複雑な形をした大きな細胞であるため,ヒトや,マウスなどの大型の実験モデル動物では細胞の全体像を捉えることが難しく,ALS研究の障壁となっている。一方で,体が小さくて透明に近いゼブラフィッシュは運動ニューロンの観察に適している。
研究グループが,過去10年にわたって独自に開発を積み重ねてきたゼブラフィッシュの操作・観察技術により,「体の奥深くにある運動ニューロンの中のTDP-43を,光を使って遠隔操作すること」と,「それにともなって運動ニューロン全体に現れる変化を経時的に詳しく観察すること」が可能になり,今回の研究成果につながったという。
この研究によって,塊の発達に先立つTDP-43の集合(オリゴマー化)を防ぐことが,ALSの有効な治療法になると考えられるという。また,ゼブラフィッシュ ALSモデルは,このプロセスを直接観察できる非常に有用な研究材料であり,ALS創薬への応用が期待されるとしている。